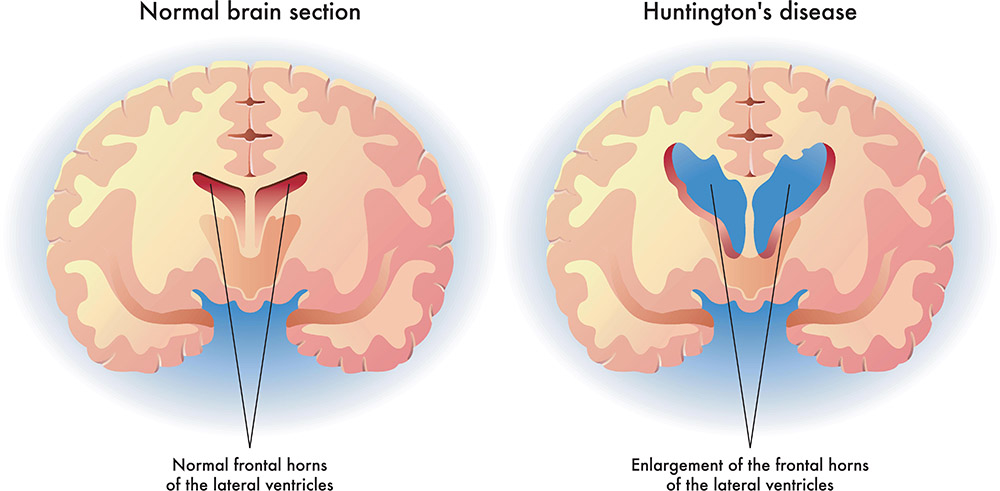
مدیریت بیماری هانتیگتون (HD)
خلاصه مقاله
بیماری هانتینگتون (HD) یک بیماری عصبی ارثی است که با علائم عصبی روانپزشکی، یک اختلال حرکتی (معمولاً choreiform) و اختلالات شناختی پیشرونده مشخص می شود.
#با_مقاله_درس_بخوانیم
مدیریت بیماری هانتیگتون (HD)
بیماری هانتینگتون (HD) یک بیماری عصبی ارثی است که با علائم عصبی روانپزشکی، یک اختلال حرکتی (معمولاً choreiform) و اختلالات شناختی پیشرونده مشخص می شود. تشخیص این بیماری معمولاً از طریق شناسایی افزایش طول تکرار CAG در ژن هانتینگتین در یک بیمار با ویژگیهای بالینی بیماری تأیید میشود.
اگرچه تشخیص معمولاً ساده است، اما ممکن است تظاهرات غیرمعمول رخ دهد و تشخیص اینکه چه زمانی فردی از یک ناقل بدون علامت به وضعیت بیماری تبدیل شده است دشوار است.
بیماران به بهترین وجه در کلینیک های تخصصی چند رشته ای مدیریت می شوند، از جمله در هنگام بررسی آزمایش ژنتیک. درمانهای کنونی علامتی هستند و عمدتاً معطوف به بیماریهای عصبی و مشکلات عصبی رفتاری هستند، اگرچه شواهد کارآزمایی پشتیبانی برای این موارد اغلب محدود است.
مهم است که افراد بیمار از حمایت های پزشکی، روانی و اجتماعی مناسب برخوردار شوند، به ویژه در هنگام انجام آزمایش های ژنتیکی پیش بینی یا تشخیصی. هیچ درمان اثبات شده ای برای اصلاح بیماری برای HD وجود ندارد و درمان در حال حاضر علامتی است. در این رابطه، شواهدی که از اثربخشی نسبی درمانها حمایت میکنند، محدود است و تصمیمهای درمانی اغلب بیشتر بر اساس تجربه پزشک است تا نتایج کارآزمایی.
✅ویژگی های بالینی
HD با سه علامت عصب روانپزشکی، اختلال حرکتی پیشرونده و زوال عقل مشخص می شود. اگرچه این بیماری ممکن است در هر سنی شروع شود، اما از مراحل معمولی عبور می کند. قبل از اینکه تغییرات شناختی اولیه ظریف اما پیشرونده، اغلب با مشکلات روانپزشکی رخ دهد؛ بیماران معمولاً برای سالها بدون علامت هستند.
این ویژگی ها با یک اختلال حرکتی، به ویژه عدم شنیدن همراه است. با پیشرفت بیماری، اختلال حرکتی پیشرفت میکند و میتواند از حالت هیپرکینتیک به حالت هیپوکینتیکتر با بدتر شدن شناخت و نوسانات خلقی تغییر کند. در کلینیک، این ویژگیها را میتوان با استفاده از مقیاس رتبهبندی بیماری هانتینگتون یکپارچه ارزیابی کرد (به صورت ابزاری استاندارد متشکل از ارزیابیهای حرکتی، شناختی، رفتاری و عملکردی و مقیاس استقلال.)
✅اختلال حرکتی
مشخصه ترین ویژگی HD حرکات کریفرم پیشرونده است که معمولاً در اوایل دوره بیماری، معمولاً در دهه چهارم یا پنجم زندگی ایجاد می شود. وجود چنین حرکاتی معمولاً برای تشخیص شروع بیماری استفاده میشود، اگرچه واضح است که ویژگیهای غیرحرکتی اغلب قبل از این نقطه رخ میدهند. سنی که در آن بیماران با HD آشکار ظاهر میشوند، ارتباط نزدیکی با طول تکرار CAG دارد، در مواردی که دیر شروع میشود، طولهای تکرار کوچکتری دارند. 55 به احتمال زیاد باعث HD نوجوانان می شود). در ابتدا، حرکات هایپرکینتیک ممکن است ظریف باشند (مثلاً حرکات بی قراری در انگشتان دست هنگام راه رفتن، یا در رختخواب در شب که توسط شریک زندگی مورد توجه قرار می گیرد)، قبل از اینکه آشکارتر شود و تمام اعضای بدن به طور متقارن تحت تأثیر قرار گیرند.
✅سایر ویژگی های بالینی
کاهش وزن تا حدی به دلیل نیازهای کالری بالا ناشی از حرکات کوریفورم مداوم است، اما ممکن است به خودی خود یک آسیب شناسی متابولیک نیز داشته باشد. همچنین این می تواند با افسردگی، بی تفاوتی و دیسفاژی تشدید شود.
اکثر بیماران مشکلات خواب مانند بی خوابی، مشکل در به خواب رفتن و خواب آلودگی بیش از حد در طول روز را نیز تجربه می کنند.
✅مدیریت بیماری HD
چندین رویکرد احتمالی اصلاح کننده بیماری، از جمله درمان با الیگونوکلئوتید ضد حس، در HD بررسی شده است، اما تا به امروز هیچ کدام نشان داده نشده است که پیشرفت بیماری را کند کند. کیفیت زندگی. مجموعه ای از توصیه ها برای مدیریت بسیاری از علائم HD اخیراً به سفارش شبکه اروپایی بیماری هانتینگتون منتشر شده است،راه هایی وجود دارد که از طریق آنها می توان به بیماران کمک کرد.
شاید مهمترین جنبه مدیریت مشارکت یک تیم چند رشته ای باشد که شامل عصب شناسان، متخصصین ژنتیک بالینی، روانشناسان اعصاب، روانپزشکان اعصاب، متخصصین تغذیه، درمانگران گفتار و زبان، فیزیوتراپیست ها، کاردرمانگران، مددکاران اجتماعی، پرستاران متخصص و هماهنگ کننده های کلینیک می باشد. گروههای حمایت از بیماران (مانند انجمن HD در انگلستان و ولز، انجمن HD آمریکا، و انجمن هانتینگتون کانادا) مهم هستند و برخی از آنها مشاوران منطقهای تامین مالی شدهاند که در جامعه با خانوادههای آسیبدیده کار میکنند.
فقدان بینش به این معنی است که گاهی اوقات بیماران تمایلی به پذیرش کمک ندارند و نظرات خانواده و مراقبین گاهی اوقات می تواند نشانه بهتری از مشکلات تجربه شده توسط بیمار باشد.
بحث در مورد برنامه ریزی مراقبت های پیشرفته قبل از ایجاد اختلال شناختی ، به ویژه با توجه به تعیین اولویت ها برای تغذیه کمکی (به عنوان مثال، قرار دادن گاستروستومی آندوسکوپی از راه پوست)، پذیرش در بیمارستان و تنظیمات مراقبت بسیار مهم است.
شواهد کمی در مورد داروهای علامت دار وجود دارد و انتخاب دارو به طور کلی به تجربه پزشک بستگی دارد.
همچنین در نظر گرفتن نحوه حمایت از بیمار با استفاده از اقدامات غیردارویی مانند اطمینان از دسترسی به بستههای مراقبتی مناسب، مکملهای غذایی، و حمایت از مسکن و مزایا بسیار مهم است. ورودی فیزیوتراپی و کاردرمانی می تواند مفید باشد، و برخی پیشنهادات وجود دارد که افزایش سطح فعالیت می تواند به حفظ عملکرد کمک کند.
این سازمان ها اطلاعات زیادی در مورد ماهیت HD و توصیه هایی در مورد زندگی با این بیماری ارائه می دهند. بسیاری از بیماران حضور در رویدادهای محلی و گروههای حمایتی را مفید میدانند و اینها ابزاری برای حفظ تماس اجتماعی برای برخی افراد است. نیازهای خانواده بیمار همیشه برای پزشکان (به ویژه کودکان، که ممکن است در قرار ملاقات حضور نداشته باشند) آشکار نیست، و گروه های حمایت از بیمار می توانند در رسیدگی به این موارد کمک کنند. وبسایت HD Buzz (https://en.hdbuzz.net) یک منبع اضافی است که اخبار تحقیقاتی HD را به زبان ساده منتشر میکند که میتواند برای بیماران و پزشکان مفید باشد.
منبع: https://pn.bmj.com/content/22/1/32.long
گردآورنده: مهدیه وحدتی نسب
مقالات مرتبط
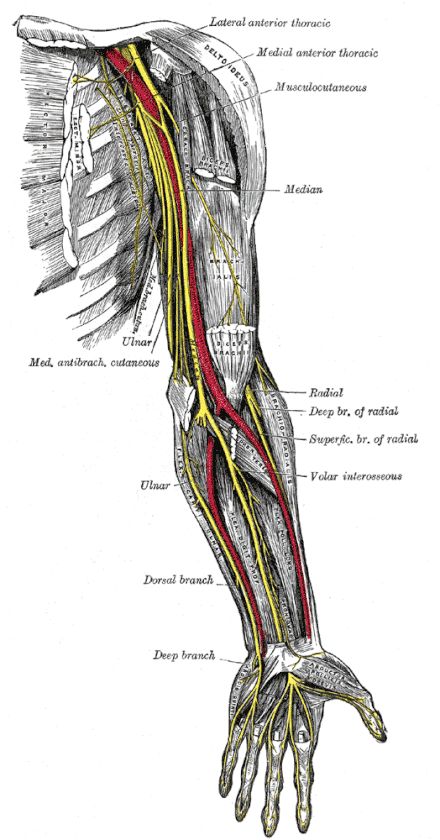
معاینه عصب و اولنار
عصب اولنار امتداد طناب داخلی شبکه بازویی است. این یک عصب مختلط است که عصب را به ماهیچه های ساعد و دست می رساند و در نیمه داخلی انگشت چهارم و کل انگشت پنجم (جنبه اولنار کف دست) و قسمت اولنار قسمت خلفی آن احساس ایجاد می کند. دست (توزیع پوستی اولنار پشتی). گیر افتادن عصب اولنار دومین نوروپاتی گیرافتاده شایع در اندام فوقانی (بعد از گیر افتادن عصب مدین) است. شایع ترین محل گیر افتادن عصب اولنار در ناحیه آرنج یا نزدیک آن است، به خصوص در ناحیه تونل کوبیتال یا در شیار اپی کندیلار (اولنار). دومین مکان محتمل در مچ دست یا نزدیک آن است، همچنین می تواند در ساعد بین این دو ناحیه، زیر مچ (دست) یا بالای آرنج رخ دهد
توماس یانگ
توماس یانگ (1773-1829) یک پزشک و فیزیکدان انگلیسی بود که اصل تداخل نور را پایه گذاری کرد و نظریه موجی نور را احیا کرد. او همچنین به رمزگشایی سنگ روزتا کمک کرد و کمک قابل توجهی به درک ادراک حسی و آستیگماتیسم کرد.