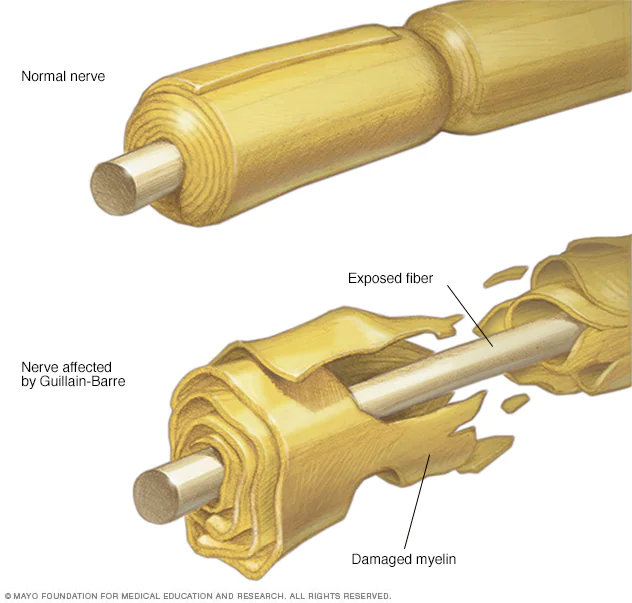
بیماری گیرن باره چیست؟
خلاصه مقاله
گیلن باره یک بیماری خطرناک پیشرنده است که
#با_مقاله_درس_بخوانیم
#Guillain_Barre_Syndrome
واکسن ها و سندروم گیلن-باره
افزایش نظارت بر سندرم گیلن باره مرتبط با تجویز واکسن به دلیل گزارشهایی مبنی بر افزایش خطر ابتلا به سندرم گیلن باره (تقریباً یک مورد از هر 100000 واکسن) در افرادی که واکسن آنفولانزای H1N1 در سال 1976 دریافت کرده بودند، انجام شد.
البته واکسیناسیون خطر ابتلا به عود را در افرادی که قبلاً به سندرم گیلن باره مبتلا شده بودند افزایش نداد.
Immune checkpoint inhibitors و سندروم گیلن-باره
با معرفی مهارکننده های ایمنی به عنوان دارو در درمان سرطان، سرطان هایی که قبلا غیر قابل درمان بودند، اکنون بهبود یافته اند. عوارض جانبی عصبی، هرچند نادر، گزارش شده است، از جمله وضعیتی شبیه به سندرم گیلن باره.
میانگین زمان شروع در بیماران مبتلا به سندرم گیلن باره معمولاً پس از سه دوره درمان با مهارکننده های ایمونولوژیک بود و پیشرفت بیماری سریع بود.
توصیه درمانی کنونی برای عوارض عصبی ناشی از درمان با مهارکننده های ایمونوتیک، توقف داروی مسبب و شروع مصرف استروئیدها است.
با این حال، از آنجایی که به نظر می رسد سیر بالینی سندرم گیلن باره ناشی از مهارکننده های ایمنی شبیه به سندرم کلاسیک گیلن باره است، ایمونوگلوبولین وریدی یا تبادل پلاسما باید در نظر گرفته شود.
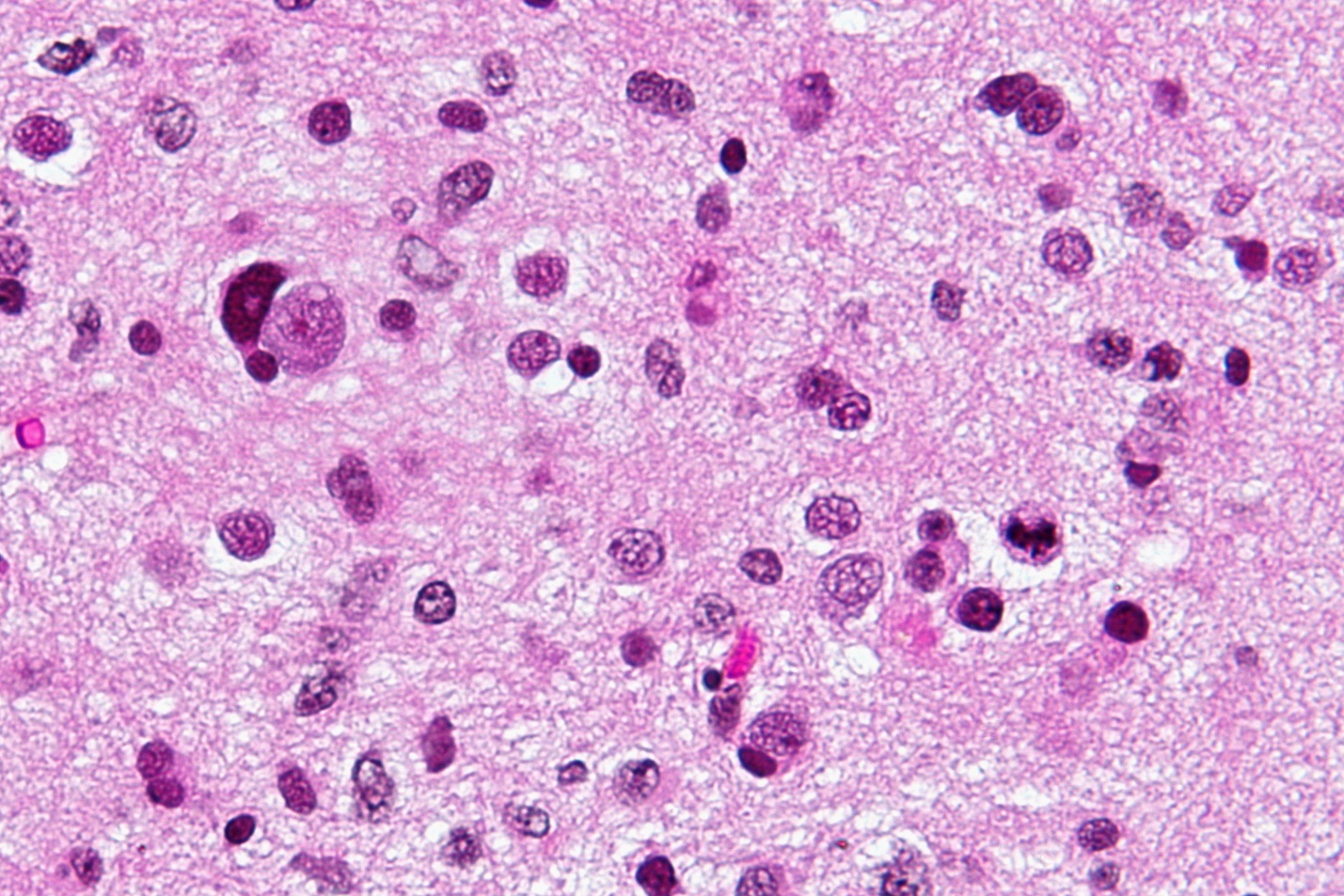
نقش آنتیبادیها
گانگلیوزیدها گلیکولیپیدهای حاوی اسید سیالیک هستند که در سیستم عصبی پستانداران، به ویژه در گره های Ranvier و پایانه های عصبی حرکتی غنی شده اند. اهمیت آنها به عنوان هدف در موشهای تراریخته نشان داده شده است که گانگلیوزیدهای پیچیده را منحصراً در نورونها بیان میکنند. مکانیسم اساسی برای نوروپاتی با واسطه آنتیبادی شامل تعدیل عملکرد کانال یونی در گرههای Ranvier، سمیت سلولی وابسته به مکمل در گرهها و پایانههای عصبی حرکتی، و تداخل با بازسازی عصبی.
زیرگروه های سندرم گیلن باره اغلب با آنتی بادی های آنتی گانگلیوزید خاص همراه هستند که نشان دهنده غنی سازی نامتناسب گلیکولیپیدهای هدف در اعصاب مختلف است.
معیارهای تشخیصی
معیارهای متعددی برای کمک به پزشکان در تشخیص سندرم گیلن باره ایجاد شده است.
حداقل، تشخیص سندرم گیلن باره مستلزم وجود ضعف متقارن شل و کاهش رفلکس در غیاب علل جایگزین است.
معیارهای برایتون همچنین تعریف مورد جداگانه ای را برای سندرم میلر فیشر در نظر می گیرد، که نیاز به حضور سه گانه بالینی افتالمپلژی دو طرفه، کاهش رفلکس ها و آتاکسی، همراه با فقدان ضعف اندام و درگیری CNS برای تحقق یک قطعیت تشخیصی سطح 3 دارد.
دستیابی به قطعیت های تشخیصی بالاتر در هر دو سندرم گیلن باره و سندرم میلر فیشر مستلزم وجود یک بیماری تک فازی است که در عرض 28 روز به حد نادر می رسد، تجزیه آلبومین سیتولوژیکی مایع مغزی نخاعی و شواهد الکترودیاگنوستیک نوروپاتی.
در عمل، ویژگی های بالینی سندرم گیلن باره متغیر است. اگرچه در هیچ یک از معیارهای تشخیصی گنجانده نشده است، یک بیماری پیشین در 4 هفته قبل در 76٪ از بیماران وجود دارد.
الگوی ضعف در سندرم گیلن باره به اندام ها نیز محدود نمی شود و می تواند شامل عضلات عصب دهی شده جمجمه، عضلات تنفسی و درگیری اتونوم شود. به ندرت، این الگوهای غیر معمول می تواند اولین تظاهر سندرم گیلن باره باشد.
امروزه هم از معیارهای تشخیصی برایتون و هم معیارهای موسسه ملی اختلالات عصبی و سکته مغزی ایالات متحده (NINDS) استفاده میشود.
گیلن باره در کودکان
تشخیص سندرم گیلن باره در کودکان می تواند چالش برانگیز باشد. با این حال، درد قابل توجهی در ارتباط با سندرم گیلن باره کودکان وجود دارد که می تواند ضعف اندام را بپوشاند و باعث تاخیر در تشخیص شود. هنگامی که مطالعات هدایت عصبی در کودکان قابل تحمل نباشد، تصویربرداری عصبی با MRI یا اولتراسوند می تواند تشخیص را تسهیل کند. کودکان مبتلا به سندرم گیلن باره پیش آگهی خوبی دارند، اما از آنجایی که گزارش هایی از مرگ و میر ناشی از اختلال عملکرد اتونوم وجود دارد، استراتژی های درمانی، همانطور که در سندرم گیلن باره بزرگسالان توصیه می شود، توصیه می شود.
گردآورنده: ساغر مومنی
ادیت:دکتر فرزان فهیم
🆔 @Neurosurgery_association
مقالات مرتبط
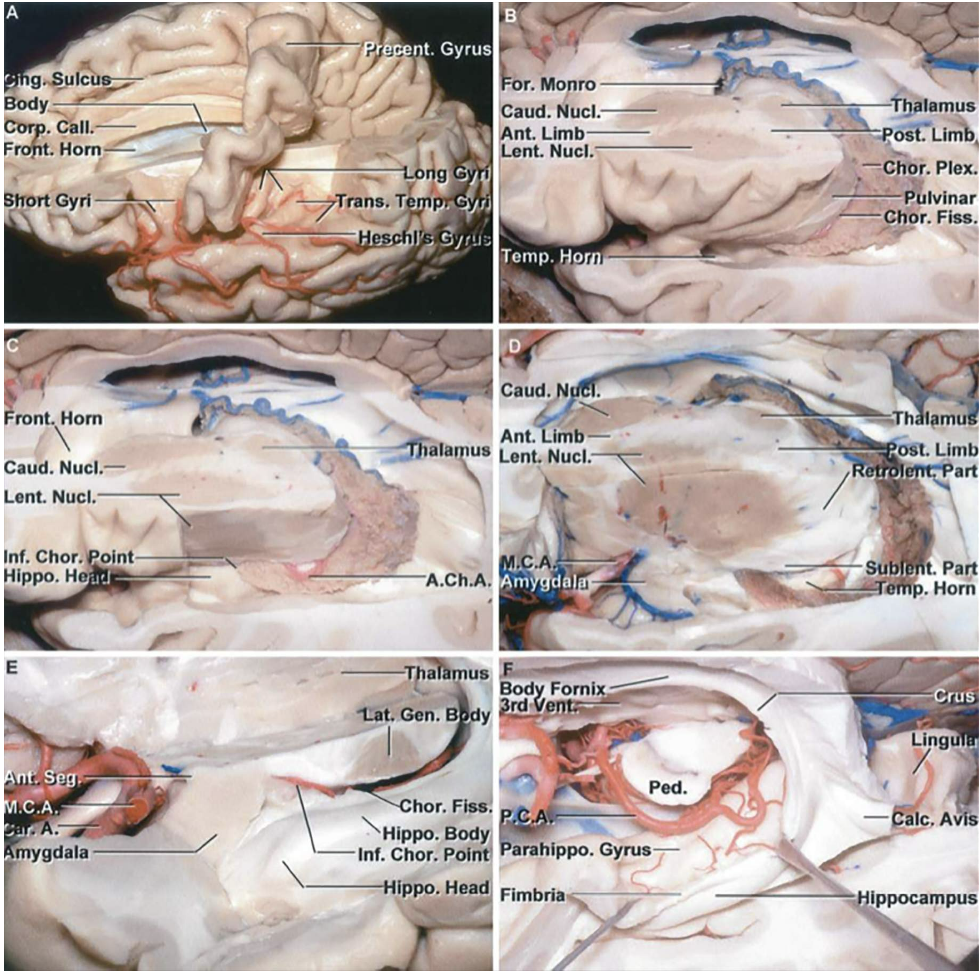
تومورهای تالاموسی
تومورهای تالاموس نادر هستند و تقریباً 5 درصد از کل تومورهای مغزی را تشکیل می دهند. در همه گروه های سنی رخ می دهد اما در کودکان شایع تر است. پیشرفتها در روشهای تصویربرداری و تکنیکهای میکروسرجری، رویکردهای هدفمند جمجمهای را ایجاد کرده است که عوارض جراحی را به حداقل میرساند و میزان ایمن برداشتن ضایعه را به حداکثر میرساند. با ادامه پیشرفت تکنیکهای جراحی میکروسکوپی، رویکردهای جراحی مؤثرتری برای تومورهای تالاموس قابل دستیابی است. علائم و نشانهها مربوط به افزایش فشار داخل جمجمه (به عنوان مثال، سردرد پیشانی، بی حالی و استفراغ) و علائم ادم پاپی می شود. قسمت داخلی هر تالاموس مرزهای جانبی بطن سوم را تشکیل می دهد. اختلال در هسته های خاص (specific nuclei) می تواند یافته های ویژهای را استخراج کند: هسته های Reticular و intralaminar - هسته های حسی - هسته های Effector - هسته های Associative - هسته لیمبیک. MRI با کنتراست، روش تشخیصی اصلی برای این تومورها است. توالی بازیابی وارونگی ضعیف شده با مایع (FLAIR) می تواند برای تومورهایی که با کنتراست تقویت نمی شوند مفید باشد. تصویربرداری (DTI) می تواند به ایجاد رابطه بین مسیر قشر نخاعی و تومورهای تالاموس، به ویژه نوع thalamopeduncular کمک کند. تومورهای اولیه تالاموس منشأ گلیالی دارند. شیمیدرمانی. برخی از جراحان بسته به تشخیص، روش stereotactic needle biopsy و درمان کمکی (adjuvant) را دنبال میکنند (2). هیدروسفالی علامت دار اغلب به مداخله جراحی برای قرار دادن شانت ventriculoperitoneal یا جراحی debulking نیاز دارد تا بتواند دینامیک مایع مغزی نخاعی native (CSF) را فعال کند. انتخاب روش مناسب به منشاء، الگوی رشد تومور در رابطه با ساختارهای طبیعی و پاتولوژی مشکوک بستگی دارد. سطح راحتی و تجربه جراح با رویکرد انتخابی نیز عامل مهمی است. روشهای جراحی متعددی، از جمله روشهای anterior interhemispheric transcallosal، transcortical transventricular، contralateral infratentorial supracerebellar، posterior interhemispheric parasplenial و transsylvian transinsular توصیف شدهاند. آناتومی ورید و تغییرات آن در اطراف superior parietal lobule باید قبل از جراحی برای مسیرهای بین نیمکره ای مورد توجه قرار گیرد. 6 ناحیه تشریحی تالاموس : منطقه 1: تومورهای تالاموس قدامی تحتانی (رویکرد زیر پیشانی سوپراکاروتید اوربیتوزیگوماتیک) روش Transrostral/Subfrontal Translamina Terminalis Approach :این رویکرد محدود به تومورهای نسبتاً کوچک تالاموس قدامی تحتانی است. رزکسیون کلی تومورهای بزرگ معمولاً مشکل ساز است و بدون عقب نشینی غیرمجاز (undue retraction) در ساختارهای عصبی عروقی طبیعی اطراف امکان پذیر نیست. این رویکرد مناسب نیست و مسیر orbitozygomatic را که در بالا مورد بحث قرار گرفت، رویکرد بهتری است. منطقه 2: تومورهای تالاموس داخلی رویکرد( Anterior Interhemispheric Transcallosal ) :مرکز تومور در ناحیه تالاموس قدامی و میانی قرار دارد و به سطح pial دیواره بطن سوم می رسد روش Suprapineal Recess/Supracerebellar Transventricular: از معایب این روش می توان به آسیب پذیری habenula، رگ Galen و quadrigeminal plate اشاره کرد. منطقه 3: تومورهای تالاموس جانبی روش (Contralateral Anterior Interhemispheric Transcallosal Approach) نتیجه از رویکرد طرف مقابل (contralateral approach)، از طریق این اپروچ یک مسیر عرضی جانبی امکان پذیر (more feasible lateral cross-court trajectory) به سمت تالاموس جانبی به دست می آید. در هنگام برداشتن ضایعات تالاموس جانبی به دلیل مجاورت نزدیک کپسول داخلی باید احتیاط کرد.
آستروسیتوم آناپلاستیک
Astrocytoma شایع ترین نوع گلیوم است که معمولاً مغز و گاهی اوقات نخاع را درگیر می کند. علت دقیق آستروسیتوم آناپلاستیک ناشناخته است.در نوروفیبروماتوز نوع I، سندرم Li-Fraumeni و توبروس اسکلروزیس با فراوانی بیشتری رخ می دهد. اکثریت قریب به اتفاق آستروسیتوم ها به فرزندان منتقل نمی شوند. تأثیر سن بر survival تنها برای 2 سال اول پس از تشخیص وجود دارد. Direct Invasion و رقابت برای اکسیژن است که منجر به آسیب hypoxic به پارانشیم طبیعی مغز می شود. رادیکال های آزاد، انتقال دهنده های عصبی و مدیاتور های التهابی نیز مسئول ایجاد اختلال در هموستاز هستند. Mass Effect ناشی از تومور نیز مسئول علائم و بالینی مختلف است. Anaplastic Astrocytoma : در بزرگسالان - فقدان تکثیر اندوتلیال - Grade III . علائم General شامل سردرد ، حالت تهوع، استفراغ، مشکلات شناختی، تغییرات شخصیتی و اختلالات راه رفتن است. علائم Focal شامل تشنج، آفازی یا نقص میدان بینایی است. تشنج در حدود 90 درصد از بیماران درجه پایین رخ می دهد. یک neurological examination کامل همیشه ضروری است. ایید محل دقیق تومورها باید با تصویربرداری عصبی انجام شود. MRI بهترین روش تصویربرداری برای تشخیص است. تا حد امکان باید از کنتراست Gadolinium استفاده شود. در صورت وجود هرگونه منع برای MRI ، ممکن است CT scan انجام شود. در صورت یافتن تومور، جراح مغز و اعصاب باید biopsy از آن را انجام دهد. Standard of care: برداشتن تومور با جراحی و به دنبال آن EBRT و temozolomide 1 تا 1.5 ساعت قبل از radiation. پس از پرتودرمانی: تموزولوماید را با دوزهای بالاتر یا PVC (پروکاربازین، لوموستین، وین کریستین). تشخیص افتراقی :Glioblastoma multiforme - Brain metastasis - Brain abscess -Oligodendroglioma - Encephalitis - Multiple sclerosis - Primary CNS lymphoma - Toxoplasmosis