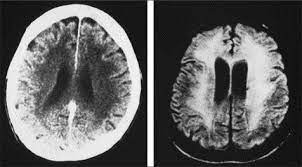
سندرم براون سکوارد به دنبال زخم ضربه خنجری به ستون فقرات قفسه سینه
خلاصه مقاله
یک مرد ۲۸ ساله با سابقه سوء مصرف مواد مخدر، پس از یک حادثه خشونت آمیز، دچار چندین آسیب شد که منجر به تشخیص سندرم برون-سیکرد (BSS) شد. سندرم برون-سکوآرد یک شکل نادر از آسیب نخاعی ناقص است که با فلج نورون حرکتی فوقانی یک طرفه و از دست دادن پریوستپشن (آگاهی از بدن) با نقص درد و حس دمای طرف مقابل ناشی از نیمسوز یا آسیب جانبی به نخاع مشخص میشود
#با_کیس_درس_بخوانیم
#سندرم_براون_سکوارد_به_دنبال_زخم_ضربه_خنجری_به_ستون_فقرات_قفسه_سینه
🔰یک مرد ۲۸ ساله با سابقه سوء مصرف مواد مخدر، پس از یک حادثه خشونت آمیز، دچار چندین آسیب شد که منجر به تشخیص سندرم برون-سیکرد (BSS) شد. سندرم برون-سکوآرد یک شکل نادر از آسیب نخاعی ناقص است که با فلج نورون حرکتی فوقانی یک طرفه و از دست دادن پریوستپشن (آگاهی از بدن) با نقص درد و حس دمای طرف مقابل ناشی از نیمسوز یا آسیب جانبی به نخاع مشخص میشود.
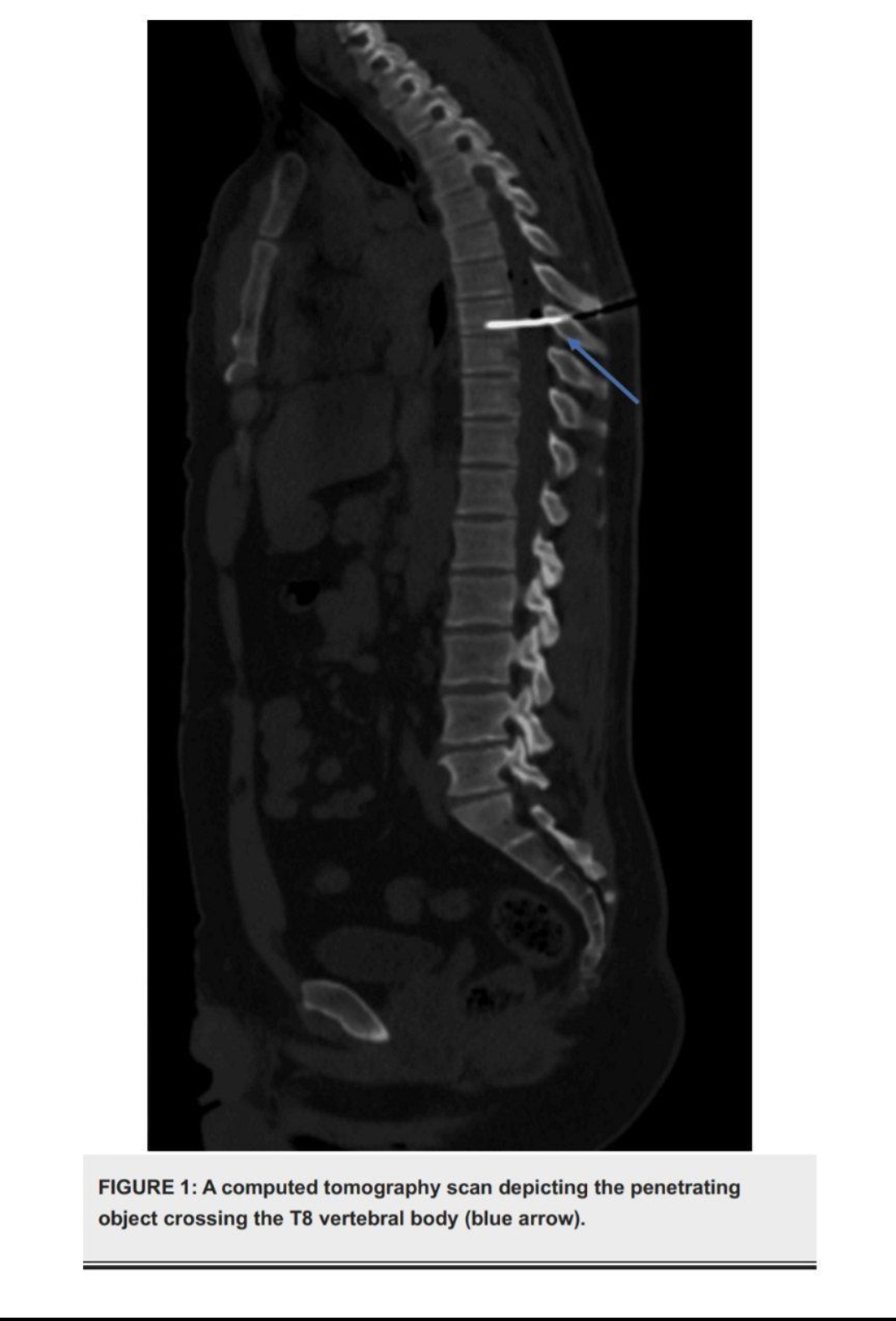
🔰بیمار هوشیار بود و به صورت رو به پایین دراز کشیده بود و یک چاقو از ستون فقرات قفسه سینهاش بیرون زده بود. تصویربرداری توموگرافی کامپیوتری (CT) مسیر چاقو را مشخص کرد و نشان داد که از فضای بینلایهای، بافت میانی نخاع و وارد بدن مهره در سطح T8 شده است و کانال نخاعی را طی میکند. با توجه به وضعیت پایدار بیمار و عدم وجود عوارض ریوی یا عروقی، مداخله جراحی مناسب تشخیص داده شد. بیمار تحت عمل جراحی فوری نوروسرجیکال برای خارج کردن سلاح تیز قرار گرفت و تصویربرداری تشدید مغناطیسی پس از عمل (MRI) نشان داد که ناحیهای با سیگنال تغییر یافته در نیممهره راست وجود دارد که به سمت چپ کشیده شده است.
🔰بیمار پس از یک آسیب نخاعی تروماتیک، با سندرم برون-سیکوآرد(BSS) تشخیص داده شد. بیمار قدرت عضلانی دستهای فوقانی خود را حفظ کرد، اما کاهش قابل توجهی در سمت راست داشت که عضلات خمکننده لگن، صافکننده زانوها و سایر عضلات خمکننده را تحت تأثیر قرار داد. کاهش حس لمسی مشاهده شد و از دست دادن پریوستپشن مشاهده شد. کنترل مثانه و روده باقی ماند.
🔰بررسی الکترومیوگرافی (EMG) نشان داد که آسیب شدید آکسونال وجود دارد که عمدتاً عصب رادیال چپ را تحت تأثیر قرار میدهد که مسئول صاف کردن مچ دست و حرکات انگشتان است. یک برنامه فشرده پزشکی فیزیکی و توانبخشی (PMR) برای ترویج بهبودی آغاز شد و یک عمل جراحی نوروررافی برای اتصال مجدد الیاف عصبی قطع شده انجام شد.
🔰بیمار برای مراقبتهای تخصصی به مدت یک ماه به یک واحد توانبخشی بستری منتقل شد. در این مدت، بیمار روزانه جلسات فیزیوتراپی، مداخلات توانبخشی حرفهای و تکنیکهای بازآموزی حسی دریافت کرد تا درک حسی را بهبود بخشد.
🔰پس از یک برنامه 30 روزه توانبخشی بستری، بیمار پیشرفت قابل توجهی نشان داد، از جمله استقلال در انتقالها (جابجایی بین وضعیت نشسته و ایستاده) و گرفتن قوی کف دست در دست چپ. بیمار سپس به یک مرکز توانبخشی دیگر منتقل شد تا روند بهبودی خود را ادامه دهد.
📚 گرد آورنده: دکتر آسیه کفاشباشی
📎 منبع
✨شکوه دنیای اعصاب در انجمن علمی دانشجویی جراحی اعصاب
با ما همراه باشید.✨
🆔English:@NeurosurgeryAssociation
🆔Persian:@Neurosurgery_Association
مقالات مرتبط
تظاهرات عصبی عفونت حاد HIV
در جمعیتهای جدید تبدیل سرمی شیوع بالایی از نوروپاتی محیطی و اختلال عملکرد شناختی در AHIV(acut hiv ) را نشان میدهد، حتی اگر این یافتهها به طور کلاسیک با عفونت مزمن HIV مرتبط باشد. آزمایشهای تشخیصی مراقبتی محدود برای AHI و تشخیص تأخیری عفونت همچنان منجر به عدم شناسایی و گزارش کم تظاهرات عصبی AHI میشود. AHI باید برای طیف وسیعی از شرایط عصبی، از فلج بل، متفاوت باشد. درمان این شرایط شامل شروع زودهنگام درمان ضد رتروویروسی (ART) و سپس درمانهای استاندارد ارائه خاص است. مننژیت آسپتیک، که عموماً با سردرد و علائم مننژی تظاهر میکند، شایعترین تظاهرات CNS AHI است که در عرض 2 هفته پس از عفونت رخ دهد. علائم اکستراپیرامیدال ظریف، مانند برادیکینزی، از شایعترین علائم مشاهده شده در معاینه عصبی طی دوازده هفته پس از عفونت HIV بود . تظاهرات سیستم عصبی محیطی HIV نیز در عفونت حاد دیده می شود. فلج مجزای عصب جمجمه ای 7 (بل) به عنوان علامت های اولیه و حتی اولین علامت مشخص با شروع متوسط 15 روز پس از تظاهرات بالینی بیماری و همیشه همراه با مننژیت آسپتیک. شایعترین علامت عصبی در 12 هفته اول عفونت HIV مشاهده شد، نوروپاتی وابسته به طول بود. فلج بل را می توان با یک دوره کوتاه کورتیکواستروئیدی و آسیکلوویر درمان کرد و AIDP با یک دوره IVIG درمان می شود. پیوند مغز استخوان (BMT) و استراتژی "شوک و کشتن" برای درمان اچ آی وی در انسان مورد مطالعه قرار گرفته است. چندین استراتژی درمانی بالقوه دیگر در حال حاضر در شرایط آزمایشگاهی در حال بررسی هستند، اگرچه آنها دور از آزمایش انسانی هستند.
تومور های هیپوفیزی عملکردی
آدنوماهای هیپوفیزی تودههای رشدیافتهای از سلولهای مونوکلونال با علائم تولید بیش از حد هورمونی، با یا بدون پرزانتاسیون عصبی هستند. پرولاکتینوماها، آدنوماهای غیرعملکردی هیپوفیز، آدنوماهای تولیدکنندهی هورمون رشد، آدنوماهای تولیدکنندهی هورمون آدرنوکورتیکوتروپین، آدنوماهای مولد هورمون تحریککنندهی تیرویید، آدنوماهای تولیدکنندهی گنادوتروپین و اینسیدنتالوماها نمونههایی از تومورهای هیپوفیزیاند. آدنوماهای هیپوفیزی براساس سایز به دستهی میکروآدنوم با سایز کمتر از یک میلیمتر و ماکرو آدنوم تقسیم میشوند.تومورهای منشا رده سلولی Pit-1 , مسوول تولید بیش از حد هورمون ادرنوکورتیکوتروپین اند. تومور های منشا رده سلولی TPIT ,با رشد خوشخیم و تولید بیش از حد هورمون رشد, پرولاکتین وTSH همراه اند. عملکرد بیش از حد گنادوتروپین ممکن است با علائم اثر تودهای، هیپوفیز یا حتی بدون علامت ظاهر شود. تشخیص بر اساس علائم بالینی است. اگر نشانهای از ترشح بیش از حد هورمون هیپوفیز وجود داشته باشد، آدنوم باید خارج شود.پانل هورمونی :پرولاکتین سرم، فاکتور رشد شبه انسولین 1 ، تست عملکرد تیروئید، همورمون لوتئینیزهکننده، هورمون تحریک فولیکولی، ارزیابی کورتیزول با آزمایش کورتیزول ۲۴ ساعته ادرار ، کورتیزول بزاق اواخر شب و سرکوب دگزامتازون است. اگر پرولاکتین سرم بیش از ۲۵۰ میکروگرم در لیتر باشد، احتمالات : پرولاکتینوما، کم کاری تیروئید، اثرات فشاری آدنوم کمعملکرد، بارداری و نارسایی کلیوی باید در نظر گرفته شود.همه بیماران با یا بدون علائم بینایی، یا با درگیری عصب بینایی در تصویربرداری باید تحت ارزیابی کامل میدان بینایی قرار گیرند. درگیری عصب جمجمه و علائم عصبی، شک به توده جمجمه را ایجاد میکند و MRI با یا بدون کنتراست گادولینیوم اجباری است. در صورت منع مصرف MRI یا CT برش نازک از مغز انجام می گردد. درمان جراحی ترانس اسفنوئیدال برای کاهش حجم توده ، رادیوتراپی و دارودرمانیبیشتر پرولاکتینومها با کابرگولین و بروموکریپتین (بیماران باردار) است. جراحی در آدنومهای تولید بیش از حد آدرنوکورتیکوتروپین مؤثر، اما در موارد غیر قابل تحمل، کتوکونازول، متیراپون و میفپریستون کاهش دهنده علائم هستند. اکترئوتید و لانروتید برای مهار هورمونهای رشد استفاده و در آکرومگالی، پگوویزومانت مفید است.